Define-se balanço de oxigênio de um explosivo, expresso em percentagem, como a massa de oxigênio faltante (sinal negativo) ou em excesso (sinal positivo), desse explosivo, para transformar todo o carbono, se houver, em gás carbônico e todo o hidrogênio, se houver, em água, dividida pela massa molar do explosivo e multiplicada por 100. O gráfico abaixo traz o calor liberado na decomposição de diversos explosivos, em função de seu balanço de oxigênio. 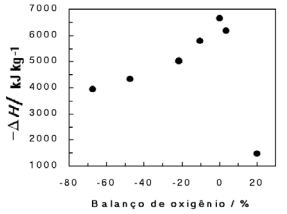


Um desses explosivos é o tetranitrato de pentaeritritol (PETN, C₅H₈N₄O₁₂). A equação química da decomposição desse explosivo pode ser obtida, seguindo-se as seguintes regras:
- Átomos de carbono são convertidos em monóxido de carbono.
- Se sobrar oxigênio, hidrogênio é convertido em água.
- Se ainda sobrar oxigênio, monóxido de carbono é convertido em dióxido de carbono.
- Todo o nitrogênio é convertido em nitrogênio gasoso diatômico.
a) Escreva a equação química balanceada para a decomposição do PETN.
b) Calcule, para o PETN, o balanço de oxigênio.
c) Calcule o ∆H de decomposição do PETN, utilizando as entalpias de formação das substâncias envolvidas nessa transformação.
d) Que conclusão é possível tirar, do gráfico apresentado, relacionando calor liberado na decomposição de um explosivo e seu balanço de oxigênio?
