Dois recipientes idênticos, um contendo palha de aço e o outro bicarbonato de sódio, foram pesados. Ambos apresentaram o mesmo valor de massa X, conforme mostram as figuras.
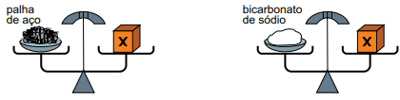
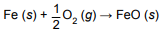
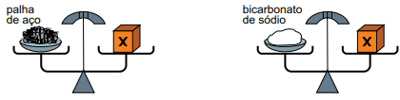
Na sequência, foram realizados dois experimentos.
Experimento 1: a palha de aço foi retirada do recipiente e submetida à combustão na chama do bico de Bunsen; o produto da reação foi retornado ao recipiente de origem que, colocado na balança, apresentou o valor de massa Y. A reação é representada na equação:
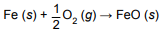
Experimento 2: o recipiente contendo bicarbonato de sódio foi inserido, aberto, em uma estufa aquecida a 140ºC, onde permaneceu por 30 minutos. O recipiente contendo o produto da reação foi colocado na balança, apresentando o valor de massa Z. A reação é representada na equação:
2NaHCO₃ (s) → Na₂CO₃ (s) + H₂O (g) + CO₂ (g)
a) Para o experimento 1, faça um esquema da balança de dois pratos, desenhando no prato esquerdo o recipiente contendo o produto da reação e no prato direito o cubo de massa X, de modo que se possa perceber claramente o desequilíbrio da balança. Faça o esquema também para o experimento 2.
b) Como podemos determinar a massa dos gases no experimento 2? Qual é a lei ponderal que justifica o cálculo proposto?