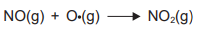
Embora as variações de entalpia tenham sido medidas e organizadas em tabelas, é possível calcular a variação de entalpia de reação, ΔH, para uma reação a partir de valores de variação de entalpia tabelados. Assim, não é necessário fazer medições calorimétricas para todas as reações químicas. Dessa forma, o cálculo da variação de entalpia para a equação química que representa a reação entre o óxido de nitrogênio (II), NO(g), com o oxigênio atômico, 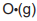 , pode ser feito com base nas variações de entalpia das equações termoquímicas
, pode ser feito com base nas variações de entalpia das equações termoquímicas
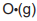 , pode ser feito com base nas variações de entalpia das equações termoquímicas
, pode ser feito com base nas variações de entalpia das equações termoquímicasI. NO(g) + O₃(g) → NO₂(g) + O₂(g) ΔHº = –198,9kJ
II. O₃(g) → 3/2 O₂(g) ΔHº = –143,3kJ
III. O₂(g) → 2 O (g) ΔHº = 495,0kJ
A partir dessas considerações sobre a variação de entalpia de uma reação química, é correto afirmar:
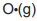 é igual a −551,6kJ.
é igual a −551,6kJ.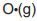 , depende apenas da energia dos reagentes.
, depende apenas da energia dos reagentes.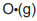 .
.