FOLHA DE DADOS

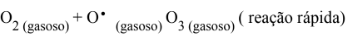
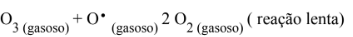
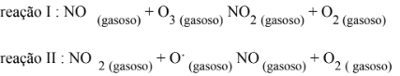
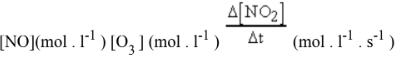
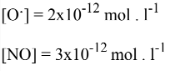
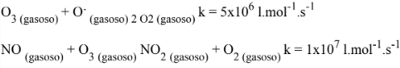

II ) R = 0,082 atm l / mol K = 2,0 cal/mol K
III ) Números atômicos e de massa
₁H¹, ₇N¹⁴, ₈O¹⁶, ₁₁Na²³, ₁₆S³², ₁₉K³⁹, ₂₅Mn⁵⁵, ₆C¹², ₃₅Br⁸⁰
IV ) 01 Faraday (F) = 96500 Coulombs (C)
A decomposição de moléculas de ozônio representa um processo natural, agravado pela interferência do homem na composição química da atmosfera. O processo natural ocorre em altitudes elevadas, como decorrência da colisão entre moléculas e átomos, segundo o mecanismo abaixo:
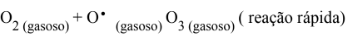
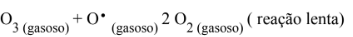
A poluição atmosférica, decorrente da emissão de gases utilizados em motores, além dos efeitos diretos causados ao homem, altera a composição dos gases na atmosfera, causando a decomposição do ozônio, segundo o mecanismo abaixo:
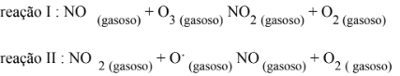
A reação I acima foi estudada em laboratório, na temperatura de 25C, apresentando os seguintes resultados:
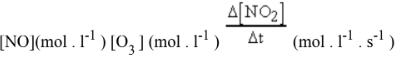
1,00 x 10⁻⁶ 3,00 x 10⁻⁶ 0,66 x 10⁻⁴
1,00 x 10⁻⁶ 6,00 x 10⁻⁶ 1,32 x 10⁻⁴
1,00 x 10⁻⁶ 9,00 x 10⁻⁶ 1,98 x 10⁻⁴
2,00 x 10⁻⁶ 9,00 x 10⁻⁶ 3,96 x 10⁻⁴
3,00 x 10⁻⁶ 9,00 x 10⁻⁶ 5,94 x 10⁻⁴
Responda aos itens abaixo:
a ) qual é o valor da constante da velocidade e a ordem global para a reação I do mecanismo de decomposição do ozônio, resultante da poluição atmosférica, calculados a 25C?
b ) qual é o papel desempenhado pelo NO (gasoso) na decomposição do ozônio?
c ) de quanto será a variação da velocidade de decomposição natural de ozônio, se a concentração de O₂ (gasoso) dobrar de valor?
d ) pela comparação dos dois mecanismos de decomposição do ozônio, através da expressão da velocidade de suas reações mais importantes , explique por que a poluição representa um risco à camada de ozônio?
Considere os dados abaixo, tomados a 40 km de altitude :
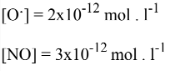
reações a serem consideradas: