A Química do Slime
A jornada histórica do slime tem início nas primeiras décadas do século XX, quando James Wright criou um material com características muito parecidas com a borracha. Atualmente, devido às mais variadas formulações disponibilizadas em plataformas e mídias digitais, pode-se produzir o próprio slime em casa.
O slime caseiro pode ser produzido pela mistura de duas colheres de chá de bicarbonato de sódio (NaHCO₃), 100 mL de água boricada (solução de ácido bórico, H₃BO₃) e 60 g de cola de isopor (constituída de poliacetato de vinila, PVAc). Quando misturamos o bicarbonato de sódio com o ácido bórico, ocorre uma reação química que produz gás carbônico, água e borato de sódio (Na₃BO₃).
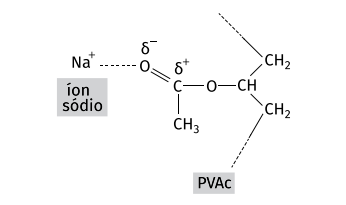
A dissociação, em solução aquosa, do borato e do bicarbonato de sódio libera íons sódio (Na⁺), que vão interagir com as moléculas do PVAc, formando um composto de elevada viscosidade e elasticidade.
Os íons sódio interagem com a estrutura do PVAc conforme representado.

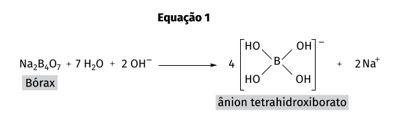
A reação entre o ácido bórico e o bicarbonato de sódio também origina o tetraborato de sódio, conhecido como “Bórax” (Na₂B₄O₇). Este, em meio básico, transforma-se em tetrahidroxiborato, conforme representado na equação 1.

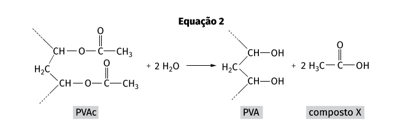
O PVAc reage com moléculas de água produzindo álcool polivinílico (PVA), conforme representado na equação 2.

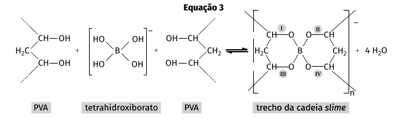
O tetrahidroxiborato reage com o PVA (equação 3), formando novas ligações que interligam as cadeias do polímero que constitui o slime.

<https://tinyurl.com/y4vmmd9w> Acesso em: 01.10.2019. Adaptado.
Na equação 3, as ligações químicas I, II, III e IV, formadas no trecho da cadeia do slime, são denominadas