(SOMATÓRIA)
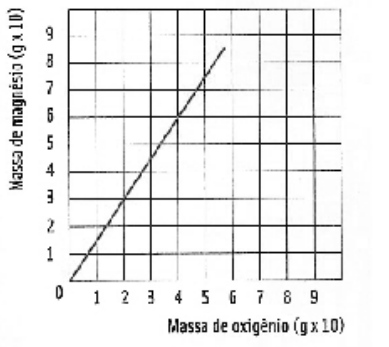
O gráfico a seguir relaciona as massas de magnésio que reagem com o oxigênio para formar o óxido de magnésio. Considerando- se essa reação como completa, ocorrida com reagentes puros, e analisando o gráfico abaixo, assinale o que for correto.
Dados: Mg = 24 g/mol; O = 16 g/mol

01) Se na reação forem utilizados 60 g de magnésio e 60 g de oxigênio, haverá um excesso de 20 g de oxigênio.
02) A proporção entre as massas de magnésio e de oxigênio que reagem para formar o óxido de magnésio é de 3 de magnésio para 2 de oxigênio.
04) Se na reação forem utilizados 60 g de magnésio e 60 g de oxigênio, haverá a formação de 120 g de óxido de magnésio.
08) A reação balanceada é a seguinte: Mg(s) + O₂(g) ---> MgO₂(s)