Soluções aquosas de compostos iônicos conduzem corrente elétrica devido à presença de íons “livres” em água. Este fato pode ser verificado através do experimento esquematizado na figura I.
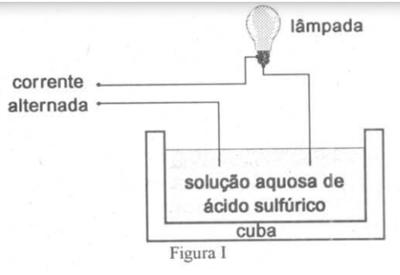


O gráfico da figura II mostra a variação da luminosidade da lâmpada em função da adição contínua de água de barita (solução aquosa de hidróxido de bário, Ba(OH)2) à solução de ácido sulfúrico na cuba. Explique o fenômeno observado.
Dados:
Ba²⁺(aq) + SO₄²⁻(aq) = BaSO₄(s); Ks = 1,0x10⁻¹⁰ (mol/L)²
Considerar o Ba(OH)₂ totalmente dissociado em solução aquosa.
Figura II
