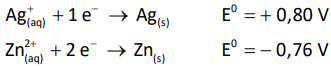Visando a determinar o produto de solubilidade do brometo de prata (AgBr), um sal praticamente insolúvel em água, um professor de Química montou um sistema, em que um potenciômetro foi colocado entre dois eletrodos, sendo um eletrodo de zinco em condições padrão e um eletrodo formado por uma placa de prata metálica imersa em uma solução aquosa, com concentração em quantidade de matéria de íons brometo igual a 0,05 mol ⋅ L⁻¹ .
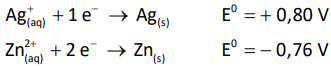
Considerando que a variação de potencial do sistema, fora das condições padrão, medida no potenciômetro, foi de 0,97 V, o produto de solubilidade do brometo de prata, a 25 ºC, é igual a
Dados:
1 F = 96500 C ⋅ mol–1;
R = 8,31 J/mol ⋅ K.
Potencial padrão de redução: