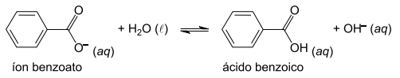
O benzoato de sódio (C₆H₅COONa) é um sal orgânico largamente empregado como conservante na indústria alimentícia. Quando dissolvido em água destilada, o íon benzoato sofre hidrólise, produzindo o ácido benzoico conforme a equação a seguir:
a) Equacione a reação que representa a dissociação aquosa do benzoato de sódio. Explique o que ocorre com a concentração de ácido benzoico no equilíbrio quando se adicionam gotas de ácido clorídrico à solução aquosa de benzoato de sódio.
b) Considerando a constante de hidrólise (Kh ) do íon benzoato igual a 2,0×10⁻¹⁰ (a 25 ºC) e considerando o produto iônico da água (Kw) igual a 1,0×10⁻¹⁴ (a 25 ºC), calcule o pH de uma solução aquosa de benzoato de sódio de concentração 0,5 mol ⋅L⁻¹, a 25 ºC.