O butano é um gás incolor, inodoro e inflamável, derivado do petróleo, utilizado como gás de cozinha.
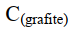 + O₂(g) → CO₂(g) ΔH⁰ = 395 kJ/mol
+ O₂(g) → CO₂(g) ΔH⁰ = 395 kJ/mol
a) Escreva a fórmula estrutural do butano.
b) Dê o nome IUPAC de um isômero do butano.
c) Escreva a equação da reação de combustão de um mol de butano devidamente balanceada.
d) A partir das equações termoquímicas mostradas a seguir, determine o valor numérico do ΔH⁰ de combustão do butano em kJ/mol.
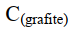 + O₂(g) → CO₂(g) ΔH⁰ = 395 kJ/mol
+ O₂(g) → CO₂(g) ΔH⁰ = 395 kJ/molH₂(g) + ½O₂(g) → H₂O(l) ΔH⁰ = 286 kJ/mol
4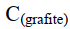 + 5H₂(g) → C₄H₁₀(g) ΔH⁰ = 126 kJ/mol
+ 5H₂(g) → C₄H₁₀(g) ΔH⁰ = 126 kJ/mol
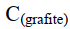 + 5H₂(g) → C₄H₁₀(g) ΔH⁰ = 126 kJ/mol
+ 5H₂(g) → C₄H₁₀(g) ΔH⁰ = 126 kJ/mol