Em uma célula voltaica a energia de Gibbs padrão de reação é determinada pela expressão:
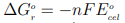

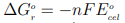
em que n é um número adimensional que representa a quantidade de mols de elétrons transferidos nas semirreações de oxidação e de redução combinadas, F é a constante de Faraday e 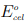 é o potencial-padrão da célula.
é o potencial-padrão da célula.
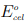 é o potencial-padrão da célula.
é o potencial-padrão da célula.Considere F = 96500 C/mol e os potenciais-padrão de redução do ferro e do alumínio, a 298 K, indicados abaixo.

Para uma célula voltaica formada pelo contato de dois metais quando uma peça de ferro é fixada com parafusos de alumínio, a 298 K, avalie as asserções a seguir.
I. O valor numérico de n é 5.
II. Com o passar do tempo, a peça fixada irá cair devido à corrosão do ferro.
III. Com o passar do tempo, a peça fixada irá cair devido à corrosão do alumínio.
IV. A energia de Gibbs padrão de reação da célula é igual a −706 kJ/mol.
V. Na célula voltaica formada, a oxidação do ferro é um processo espontâneo.
Assinale a opção que apresenta APENAS as afirmativas verdadeiras.