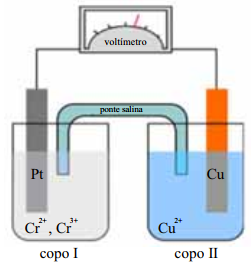
Nas células galvânicas, comumente denominadas pilhas, ocorrem reações de oxidação de redução arranjadas de forma que haja a transferência de elétrons através de um circuito externo e, assim, seja gerada corrente elétrica. A pilha representada na figura acima consiste de um eletrodo de platina mergulhado no copo I, que contém íons Cr³⁺ e Cr²⁺ em solução, e de outro eletrodo, de cobre, mergulhado no copo II, que contém uma solução de sulfato de cobre. Os potenciais padrões de redução, a 25 ºC, dos eletrodos envolvidos são apresentados abaixo.
Cr³⁺(g) + e⁻ ⇋ Cr²⁺(g)
E⁰ = – 0,41 V
Cu²⁺(g) + 2e⁻ ⇋ Cu(g)
E⁰ = + 0,34 V
Considerando essas informações e a de que a célula galvânica ilustrada está à temperatura de 25 ºC, julgue o item.
Se as soluções contidas nos copos I e II forem misturadas dentro de um mesmo copo e ambos os eletrodos forem mergulhados na solução resultante, nenhuma reação redox ocorrerá.