
O monofluorfosfato de sódio (Na₂PO₃F) é adicionado a cremes dentais para prevenção da cárie. A hidroxiapatita (Ca₅(PO₄)₃OH) do esmalte do dente é solubilizada pelos ácidos produzidos pelas bactérias da boca, o que enfraquece o esmalte. Na presença do ânion monofluorfosfato (PO₃F²⁻), parte da hidroxiapatita converte-se em fluorapatita (Ca₅(PO₄)₃F), que, por ser menos solúvel em meio ácido, torna o dente mais resistente à cárie.
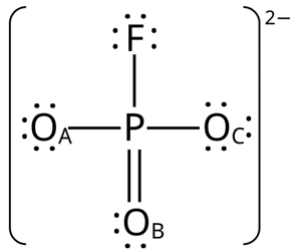
Ao se calcular as cargas formais de cada átomo na estrutura apresentada, conclui-se que são nulas, com exceção dos átomos: