Os espetáculos de fogos de artifício são mais que uma forma de entretenimento: os efeitos e as cores visualizadas resultam de reações entre diferentes sais, agentes oxidantes e redutores. Na pólvora (a carga explosiva dos fogos), agentes oxidantes, como o perclorato de potássio (KClO₄), estão misturados com agentes redutores, como o enxofre, o que é responsável pela produção da energia necessária para a explosão. A seguir, são apresentadas as equações químicas não balanceadas das reações que ocorrem no processo de explosão de determinados tipos de fogos de artifício.
reação I: KClO₄(s) → KCl(s) + O₂(g)
reação II: S(s) + O₂(g) → SO₂(g)
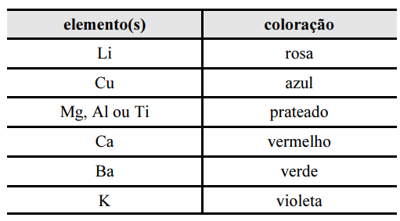
As luzes coloridas emitidas durante a queima de fogos são resultado da luminescência, fenômeno que ocorre quando os elétrons dos átomos dos sais metálicos, previamente excitados pela energia da explosão, retornam aos níveis energéticos de origem, liberando energia na forma de fótons de luz visível. A tabela a seguir mostra alguns elementos e as cores características que eles produzem na luminescência.

A partir das informações do texto, julgue o item.
Considere as seguintes informações acerca do processo de explosão de um foguete de cores: as reações I e II ocorreram em sequência, com rendimento de 100%; a energia total liberada na explosão proveio exclusivamente da queima do enxofre presente na carga explosiva; o calor de combustão do enxofre nas condições termodinâmicas do processo foi igual a 310 kJ/mol; houve a decomposição de 207,9 g de perclorato de potássio. A partir dessas informações, calcule a energia total, em kJ, liberada na explosão do foguete. Após efetuar todos os cálculos solicitados, despreze a parte fracionária do resultado final obtido, caso exista.