Em um experimento em laboratório de química, montou-se uma célula eletrolítica de acordo com o esquema:
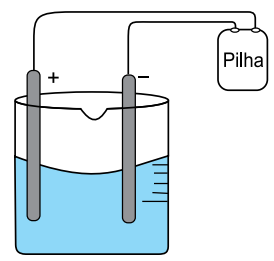
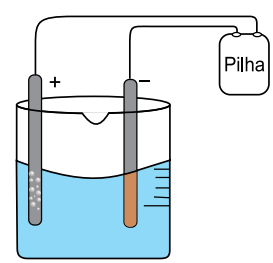

Usaram-se como eletrodo dois bastões de grafite, uma solução aquosa 1,0 mol.L⁻¹ de CuSO₄ em meio ácido a 20 °C e uma pilha.
Alguns minutos, após iniciado o experimento, observaram-se a formação de um sólido de coloração amarronzada sobre a superfície do eletrodo de polo negativo e a formação de bolhas na superfície do eletrodo de polo positivo.

Com base nos potenciais de redução a 20 °C,
Cu²⁺(aq) +2e⁻ → Cu (s) + 0,34 V
2H⁺(aq) + 2e⁻ → H₂(g) 0,00 V
O₂(g) + 4H⁺(aq) + 4e⁻ → H₂O(l) + 1,23 V
É correto afirmar que se forma cobre no