As lâmpadas de vapor de sódio emitem uma luz amarelo-alaranjada, quase perfeitamente monocromática, de comprimento de onda da ordem de 0,6 × 10⁻⁶ m. O consumo eficiente de energia elétrica e a possibilidade de controle da poluição visual nas cidades fazem com que a lâmpada de sódio esteja entre as mais empregadas na iluminação pública. Sabe-se que a emissão dessa luz característica está relacionada à estrutura do átomo: quando um elétron cai de um estado excitado para um estado de menor energia, ele libera essa diferença de energia E como um fóton de frequência f = E / h, em que h é a constante de Planck. Portanto, a radiação emitida está relacionada às transições eletrônicas possíveis em cada átomo. A figura a seguir mostra os níveis de energia dos elétrons no átomo de sódio relacionados aos níveis eletrônicos s, p, d, f.
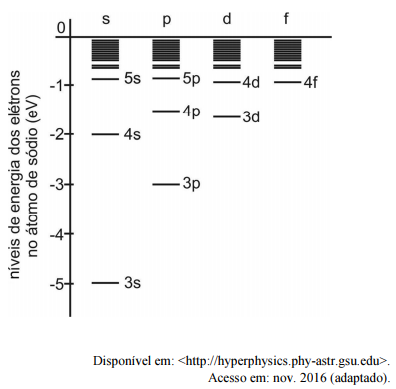

Considerando que a constante de Planck e a velocidade da luz sejam 4,0 × 10⁻¹⁵ e V⋅s e 3,0 × 10⁸ m/s, respectivamente, qual(is) a(s) transição(ões) eletrônica(s) responsável(is) pelo brilho amarelo-alaranjado da lâmpada de sódio?