Em metalurgia, um dos processos de purificação de metais é a eletrodeposição. Esse processo é representado pelo esquema abaixo, no qual dois eletrodos inertes são colocados em um recipiente que contém solução aquosa de NiCl₂.
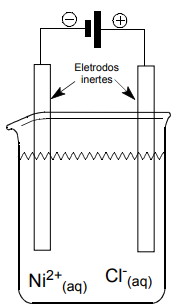

Dados:
Constante de Faraday: 96.500 C/mol
Massa Molar do Ni: 59 g/mol
Baseando-se no esquema apresentado,
a) escreva as semirreações, que ocorrem no cátodo e no ânodo, e calcule a corrente elétrica necessária para depositar 30 g de Ni(s) em um dos eletrodos durante um período de uma hora;
b) calcule a massa de NiCl₂, com excesso de 50%, necessária para garantir a eletrodeposição de 30 g de Ni(s).