A figura abaixo mostra valores de pH medidos para a chuva ácida, chuva normal e água pura.
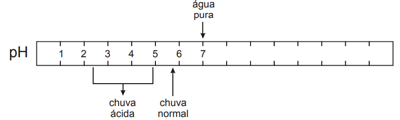

O pH da chuva normal é ácido (pH=5,6) devido, principalmente, às seguintes reações:
(1) CO₂(g) + H₂O(l) ⇄ H₂CO₃(aq)
(2) H₂CO₃(aq) ⇄ H⁺(aq) + HCO₃⁻(aq) Ka₁ ≅ 4,0 x 10⁻⁷
No caso da chuva ácida, além do CO2, contribuem para a acidez o SO3 e o NO2. As reações abaixo mostram como esses gases, em contato com a água, produzem ácidos e as respectivas ionizações desses ácidos:
(3) SO₃(g) + H₂O(l) ⇄ H₂SO₄(aq)
(4) H₂SO₄(aq) ⇄ H⁺(aq) + HSO₄⁻(aq) Ka₁ ≅ 10
(5) 4NO₂(g) + 2H₂O(l) + O₂(g) ⇄ 4HNO₃(aq)
(6) HNO₃(aq) → H⁺(aq) + NO₃⁻(aq)
Em relação aos compostos mostrados acima, é correto afirmar: