A reação 2NO(g) + 2H₂(g) ↔ 2N₂(g) +2H₂O(g) foi estudada a 904 °C. Os dados da tabela seguinte referem-se a esta reação.
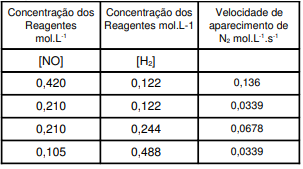

Com base na tabela acima analise as afirmações a seguir:
I) A expressão de velocidade para a equação química global é representada por V = k[NO]² [H₂], a constante de velocidade a 904C é de 0,16 molL1s1
II) A velocidade de formação de N2 é metade à velocidade de desaparecimento de H₂
III) Duplicando-se a concentração molar de NO(g) a velocidade da reação quadruplica.
IV) A velocidade das reações químicas endotérmicas aumenta com a elevação da temperatura.
Quais estão corretas?