A reação entre peças de ferro e soluções ácidas, como o ácido clorídrico, levam à formação de gás hidrogênio como um dos produtos.
2 𝐹𝑒 (𝑠) + 6 𝐻𝐶𝑙 (𝑎𝑞) ⟶ 2 𝐹𝑒𝐶𝑙₃(𝑎𝑞)+3 𝐻₂ (𝑔)
Uma forma de acompanhar a velocidade dessa reação é medindo a quantidade de gás liberado ao longo do tempo.
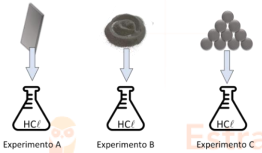
Experimentos foram feitos para estudar a reação entre uma solução ácida e diferentes objetos de ferro, sendo utilizados uma placa, esferas e pó de ferro. Manteve-se a temperatura, a pressão e a concentração de HCℓ constantes para os experimentos A, B e C.

Após a realização desses experimentos, foi verificado que um deles liberava uma baixa quantidade de gás hidrogênio, assim, esse teste foi repetido sob aquecimento, sendo denominado como Experimento D.
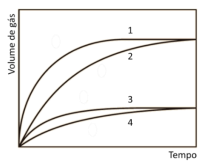
O gráfico abaixo mostra os volumes de gás hidrogênio desprendidos durante os experimentos descritos em função do tempo.

Sobre esses experimentos, é possível afirmar: