A solubilidade de algumas substâncias pode ser alterada com o pH do meio. Um exemplo pode ser observado no gráfico abaixo, que representa a variação da solubilidade dos sólidos Fe(OH)₃(s) e Al(OH)₃(s) em função do pH. Assim, em pH = 2,5 tem-se Fe(OH)₃(s) e em pH = 1,0, este hidróxido solubiliza-se.
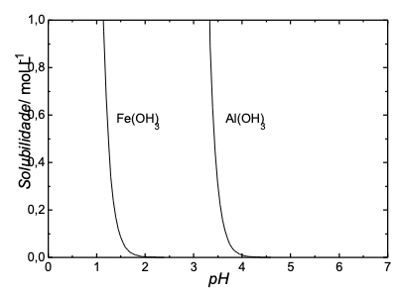

a) Considere uma solução de Al³⁺(aq), de concentração 0,2 mol/L. A partir de que pH começará a haver precipitação do Al(OH)₃(s)?
b) Sugira um valor ou um intervalo de pH adequado para precipitar apenas uma das duas substâncias e diga qual será a substância a ser precipitada.
c) Adicionando-se 0,2 mol de cada um desses dois hidróxidos em 1,0 litro de água pura, será observada a solubilização dos mesmos? Justifique a sua resposta.