Em toda situação de confinamento, prevista ou acidental, como no recente desastre na mina de cobre do Chile, sempre há grande preocupação com a revitalização do ar ambiente. O superóxido de potássio (KO₂) pode ser utilizado em dispositivos para revitalização do ar ambiente, já que ele reage com o gás carbônico, eliminando-o, e formando oxigênio gasoso como produto.
a) As equações das reações que ocorrem com o KO2 em ambiente seco e úmido são, respectivamente,
4KO₂(s) +2CO₂(g)=3O₂(g)+2K₂CO₃(s) e
4 KO₂(s) + 4 CO₂(g) + 2 H₂O(g) = 3 O₂(g) + 4 KHCO₃(s)
Em qual dos casos (ambiente seco ou úmido) um dispositivo contendo dióxido de potássio seria mais eficiente para o propósito a que se destina? Justifique.
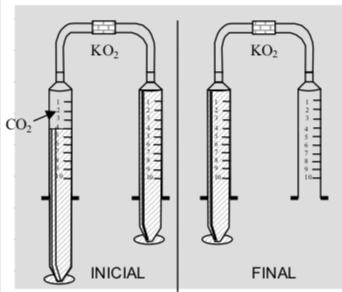
b) O esquema abaixo é de um experimento que simula a situação de confinamento. À esquerda encontra-se a fase inicial e à direita, a final. No experimento, o êmbolo contendo CO₂ é pressionado, fazendo esse gás reagir com o KO₂. Levando em conta a estequiometria da reação, complete a situação final, desenhando e posicionando corretamente o êmbolo que falta. Justifique sua resposta, considerando que a reação é completa e só ocorre enquanto o êmbolo é empurrado, que a temperatura é constante e que não há atrito no movimento dos êmbolos.
