A Primeira Lei da Termodinâmica parte do princípio de conservação de energia em um sistema termodinâmico. Por meio de fórmulas matemáticas e embasamento teórico, essa lei versa sobre a variação da energia interna de um sistema, depois que ele realizou trabalho, também mensurando a quantidade de calor absorvida.
Continue lendo este artigo e entenda melhor a definição e as aplicações da Primeira Lei da Termodinâmica, tanto em termos de fórmula, como em questões de vestibulares que cobram esse tema.
Navegue pelo conteúdo
Como é a Primeira Lei da Termodinâmica?
Para entender melhor a Primeira Lei da Termodinâmica, é preciso ter em mente o Princípio da Conservação das Energia, muito importante para diversas áreas da Física.
Esse princípio que rege os estudos físicos transmite a ideia de que, em um sistema termodinâmico, a energia nunca “some”: ela pode ser perdida para o meio em que se encontra, absorvida ou transformada por um corpo, mas sempre se mantém na mesma quantidade.
A partir disso, a Primeira Lei da Termodinâmica aparece com uma formulação matemática que resume essas informações. Ela trata de três grandes conceitos, que estão muito presentes nas máquinas térmicas: energia interna (U), trabalho (?) e calor(Q).
A energia interna de um corpo é aquela que está presente no movimento e posição dos átomos e moléculas que o constituem.
Como sabemos da química, quando um corpo ganha temperatura, as partículas atômicas tornam-se mais agitadas, por isso a energia interna desse objeto estará aumentando. Do lado oposto, quando a temperatura decresce, a movimentação dos átomos diminui e a energia interna será menor.
O trabalho realizado por um corpo diz respeito a uma transferência de energia com geração de uma força. Por exemplo, em máquinas a vapor, o trabalho resulta na movimentação dos pistões — causada pela expansão do vapor dentro do sistema.
Por fim, a definição de calor é a energia em trânsito em um ambiente. A nível de vestibular, essa grandeza é estudada pela calorimetria, dada sua influência nos estados físicos de um material, principalmente.
Fórmula da 1ª Lei da Termodinâmica
Agora que você já conhece todas os conceitos fundamentais para o entendimento da Primeira Lei da Termodinâmica, veja a fórmula que resume todas essas ideias:
ΔU = Q – ?
ΔU é a variação da energia interna, medida em calorias (cal) ou Joules (J)
Q é a medida do calor, nas unidades de calorias (cal) ou Joules (J)
? é o trabalho, também medido calorias (cal) ou Joules (J)
A fórmula transmite uma só ideia: “A variação da energia interna de um corpo é dada pela diferença entre a quantidade de calor que ele recebeu, menos a quantidade de energia que foi transferida para o meio em forma de trabalho realizado”.
Para elucidar: imagine que uma máquina térmica recebeu um calor de 1200J. A partir disso, foi gerado vapor, que se expandiu e movimentou um pistão, com um trabalho de 700J.
Note que ainda vão sobrar 1200 – 700 = 500J (quinhentos Joules) para o corpo. Isso significa que ele absorverá essa “sobra” em forma de energia interna, por isso a variação da energia interna será ΔU=500J.
Entender o que isso significa também é importante para as aplicações da fórmula da Primeira Lei da Termodinâmica:
Quando ΔU>0, o corpo ficou com uma quantidade a mais de calor depois de todo o processo, ou seja, sua temperatura subiu.
Se ΔU<0, significa que o corpo recebeu uma quantidade de calor menor do que o necessário para a realização do trabalho. Assim, ele cedeu mais energia do que recebeu, ou seja, sua temperatura diminuiu.
Quando Q>0, significa que o corpo está absorvendo/recebendo calor do meio externo. Entretanto, se Q<0, ele está enviando calor para o ambiente em que está inserido.
Nos casos em que o sistema expande, o ?>0 e ele está realizando trabalho sobre o meio. Mas nas situações em que o sistema sofre contração do meio: ?<0.
Tabela para a Primeira Lei da Termodinâmica
Veja, na tabela abaixo, um resumo sobre o comportamento de cada grandeza em situações diferentes:
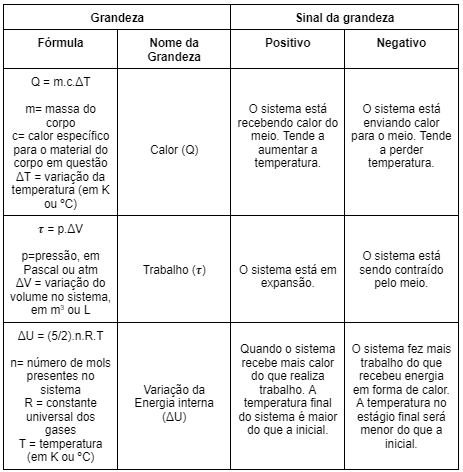
+ Veja também: Diagrama de Fases: o que é e como interpretar
Questão de vestibular sobre a 1ª Lei da Termodinâmica
Vamos resolver juntos uma questão sobre a Primeira Lei da Termodinâmica?
UECE 2015
Em um motor de carro convencional a primeira transformação de energia em trabalho ocorre dentro do cilindro que aloja o pistão. De modo simplificado, pode-se entender esse sistema como um cilindro fechado contendo um êmbolo móvel, que é o pistão. Em um dado instante a mistura ar e combustível sofre combustão forçando os gases resultantes dessa queima a sofrerem expansão, movimentando o pistão ao longo do eixo do cilindro.
É correto afirmar que a energia térmica contida nos gases imediatamente após a combustão é
a) parte transferida na forma de calor para o ambiente e parte convertida em energia cinética do pistão.
b) totalmente transferida como calor para o ambiente.
c) totalmente convertida em trabalho sobre o pistão.
d) parte convertida em trabalho sobre o pistão e o restante convertida em energia cinética também do pistão.
O enunciado trata, puramente, da Primeira Lei da Termodinâmica. Os gases que empurram o pistão possuem certa energia térmica, que será transferida para os pistão, gerando trabalho. Mas se lembrarmos a fórmula ΔU = Q – ?, observamos que essa energia também se altera devido a uma quantidade de calor que será perdida no ambiente.
Vale ressaltar que nenhuma máquina térmica consegue converter puramente o calor em trabalho, sem dissipação de energia para o meio. Assim, a alternativa correta é a letra A.
Treine questões de física para o vestibular!
Um bom desempenho em questões exatas depende, principalmente, de conceitos bem consolidados e do desenvolvimento de raciocínio lógico. Para treinar essas habilidades, é importante fazer muitas questões física, química e matemática. Conheça o banco de questões do Estratégia Vestibulares e tenha acesso a uma diversidade de exercícios para reforçar seu conhecimento!
Veja também:
- Leis de Newton: princípios, conceitos e aplicações
- Gravidade: o que é, valor e muito mais!
- Termodinâmica: o que é, fórmulas e leis
- Calorimetria no Enem: como cai?
- Hidrostática: pressão, densidade e fórmulas
- Princípio de Arquimedes: o que é, peso aparente e fórmulas
- Resolução da prova de Física da 2ª Fase da Unicamp 2020
- Resolução Comentada da prova de Física FUVEST 2020




