As dinâmicas de energia, as trocas de calor e os equilíbrios térmicos influenciam no cotidiano de todos os seres vivos. Por isso, a calorimetria é um ramo muito estudado da físico-química e aparece no Enem com frequência.
Para te ajudar a compreender os diversos aspectos desse tema, o Estratégia Vestibulares desenvolveu um resumo com os principais conceitos e definições calorimétricas. Confira!
Navegue pelo conteúdo
O que é calorimetria?
A calorimetria é o estudo das dinâmicas de calor que ocorrem entre os corpos. Por meio dela, é possível analisar temperaturas de equilíbrio, transferências de energia, capacidades térmicas e mudanças de estado físico.
Portanto, a calorimetria traz conceitos como as escalas termométricas, mudanças de estados — líquido, gasoso e sólido — equilíbrio térmico e outros temas.
Principais temas sobre calorimetria no Enem
O Enem cobra, todos os anos, questões sobre calorimetria. A seguir, confira os principais tópicos do assunto.
Conceitos de calor e temperatura
A temperatura é uma grandeza física que determina a agitação das moléculas. Quanto maior a excitação molecular, maior a temperatura e o contrário é verdadeiro.
O calor é uma grande física que representa a energia em transição entre os corpos. Por essa razão, esse conceito é dependente da existência de dois ou mais materiais com diferentes temperaturas.
Escalas termométricas
As escalas termométricas representam a temperatura ou energia térmica em um corpo.
As principais escalas são:
- Celsius: baseia-se nos pontos de fusão e ebulição da água, entre 0ºC a 100ºC — pode apresentar temperaturas negativas;
- Fahrenheit: graduada entre 32ºF e 212ºF — também contém valores negativos ;e
- Kelvin: determinada entre 273K e 373K — não admite valores menores do que 0K, visto que essa é a temperatura mais baixa possível (zero absoluto).
Transferências de calor
As transferências de calor acontecem quando o grau de agitação das moléculas dos corpos são diferentes. De forma geral, quanto maior a diferença entre as temperaturas, maior a velocidade de movimentação do calor.
Nesse processo, o calor flui do corpo mais quente para o mais frio e só é concluído quando as temperaturas dos corpos se igualam.
Equilíbrio térmico
Após o fim da transferência de calor entre os corpos, a temperatura dos materiais deve se igualar — esse evento é denominado de equilíbrio térmico e representa a situação ideal da calorimetria.
Calor Específico
O calor específico (c) é um valor determinado para cada substância e demonstra a capacidade de alterar sua temperatura(?), conforme sua massa (m).
Ele aparece na fórmula Q=m.c.Δ? e, geralmente, pode assumir diferentes unidades. Nas questões,o assunto se adequa de acordo com a necessidade do enunciado e pergunta.
Exemplo: calor específico da água = 1 caloria.grama/ºC
Mudanças de fase
As mudanças de estado físico estão intimamente relacionadas com a calorimetria. Conforme o calor transita entre os elementos, o grau de agitação das partículas é modificado, o que permite a alteração física.
Quando o corpo recebe calor, a mudança de fase pode ser do
- Estado sólido para o líquido; e
- Estado líquido para o gasoso.
Por outro lado, quando o material perde calor, a alteração do estado físico pode acontecer do:
- Estado gasoso para o líquido; e
- Estado líquido para o sólido.
Calor latente
Calor latente (L) é a grandeza que dimensiona a transferência de energia para a alteração do estado físico em uma substância. Na fórmula, ele aparece relacionado com a massa (m) e a quantidade de calor (Q)
Q=m.L
Quando Q>0, o material está recebendo calor para alterar o estado físico.
Quando Q<0, a substância está cedendo calor enquanto altera seu estado físico.
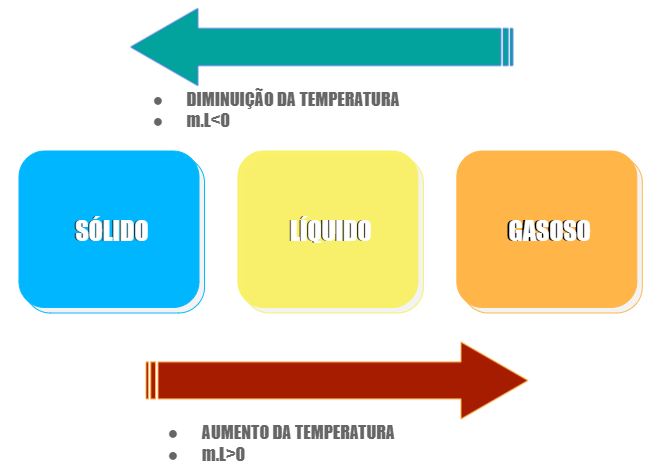
Para melhor compreensão, confira a imagem abaixo:
Questões sobre Calorimetria no Enem
Para treinar seu conhecimento sobre Calorimetria e se acostumar com o modelo das questões cobradas pelo Enem, faça o exercício a seguir e acompanhe a resolução proposta pelo Estratégia Vestibulares.
ENEM (Segunda aplicação) 2017
O aproveitamento da luz solar como fonte de energia renovável tem aumentado significativamente nos últimos anos. Uma das aplicações é o aquecimento de água(?água=1kg/L) para uso residencial. Em um local, a intensidade da radiação solar efetivamente captada por um painel solar com área de 1m² é de 0,03 kW/m². O valor do calor específico da água é igual a 4,2 kJ/(kgºC).
Nessa situação, em quanto tempo é possível aquecer 1 litro de água de 20ºC até 70ºC?
a) 490 s
b) 2800 s
c) 6300 s
d) 7000 s
e) 9800 s
Para resolver essa questão, é importante reunir e organizar todas as informações descritas pelo enunciado:
- Densidade da água: 1 kg/L
- Intensidade de radiação captada (ou potência): 0,03 kW/m2
- Área do painel: 1m2
- Calor específico da água: 4,2 kJ/(kgºC)
- Volume de água que será aquecido: 1 Litro
- Temperatura Final: 70º C
- Temperatura Inicial: 20ºC
Como o exercício aponta as unidades kJ/(kgºC), é importante converter todas as grandezas para serem iguais e facilitar as contas.
Para isso, é importante lembrar que a unidade Watts (W) representa 1 Joule por segundo. Assim, P = 0,03kW/m2 são P = 0,03 k(J/s)/m2, ou seja, P = 0,03 k.J/m2.s
Como a densidade da água é um 1kg/L e deseja-se aquecer 1L de água, a massa de água é igual a 1 quilograma. A variação da temperatura, por sua vez, compreende a diferença entre a temperatura final e inicial do líquido:
Temperaturafinal – Temperaturainicial = Δ?
70ºC – 20ºC = Δ?
Δ? = 50ºC
Dado que a questão pergunta o tempo de aquecimento com base em uma variação de temperatura e fornece o calor específico, a fórmula da calorimetria é muito útil:
Q= m.c.Δ?
Q=1.4,2.50
Q=210 kJ
Agora que já sabemos a quantidade de calor necessária para aquecer a água, é necessária uma fórmula que relacione o tempo (pedido na questão), o calor e a potência do aquecedor:
Potência = Quantidade de calor / tempo
P= Q/Δt
0,03 = 210/Δt
0,03.Δt=210
Δt=210/0,03
Δt=7000s
Note que, ao manter as unidades do calor específico e da potência, o tempo referido fica em segundos, como pede o enunciado. Dessa forma, a alternativa correta é a letra D.
Veja como o Estratégia Vestibulares pode te ajudar!
Quer saber ainda mais sobre calor, temperatura, potência e outros aspectos da calorimetria? Assista às aulas de física gratuitas do Estratégia Vestibulares no youtube:
Gostou do conteúdo e quer conhecer o material exclusivo do Estratégia? Clique no banner abaixo e conheça nossos cursos preparatórios para o vestibular, desenvolvidos para te ajudar no caminho rumo à aprovação!
Veja também:
- O que mais cai em Física no Enem?
- Ordem de grandeza: conheça os conceitos e a notação científica
- Diagrama de Fases: o que é e como interpretar
- Fórmulas de Física mais comuns do Enem e outros vestibulares
- Hidrostática: pressão, densidade e fórmulas
- Como cai a óptica no Enem
- Eletricidade: conheça as principais fórmulas e conceitos
- Resolução da prova de Física da 2ª Fase da Unicamp 2020
- Resolução Comentada da prova de Física FUVEST 2020




